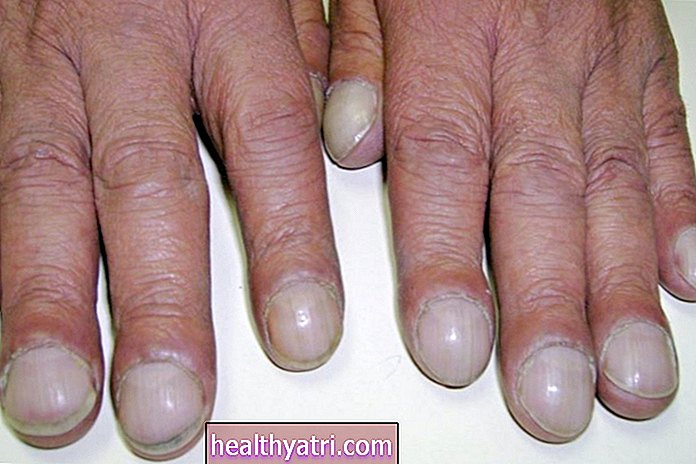
三酸化ヒ素(ATOまたはトリセノックスとしても知られています)は、急性前骨髄球性白血病(APL)として知られている急性骨髄性白血病のサブタイプに対する抗がん治療です。この白血病サブタイプは、急性骨髄性白血病の「M3サブタイプ」とも呼ばれます。
低リスクから中リスクのAPLを有する新たに診断された患者の治療にATOを使用した結果は非常に良好でした。これらの成功はまた、転移性結腸癌や脳腫瘍、多形性膠芽腫などの非白血病性悪性腫瘍を含む、APL以外の多くの癌におけるATOの潜在的な使用を調査する科学的研究に拍車をかけました。
ATOは、急性前骨髄球性白血病の治療に使用されるレチノイド剤であるオールトランスレチノイン酸(ATRA)と組み合わされることがよくあります。レチノイド化合物は、細胞の受容体に結合して、細胞のライフサイクルに重要な作用を及ぼす可能性があります。 ATRAとATOの併用は、新たに急性前骨髄球性白血病(APL)と診断された標準リスク患者の治療において、ATRAと化学療法よりも優れていることが示されています。
アリエルスケリー/ゲッティイメージズ
ATOはどのように機能しますか?
ATOの作用機序は完全には理解されていません。
ヒト前骨髄球性白血病細胞の実験室研究では、ATOは細胞の外観の変化とDNAの破壊を引き起こしました。これらは両方とも、アポトーシスまたはプログラム細胞死として知られるプロセスを示しています。
ATOはまた、前骨髄球性白血病/レチノイン酸受容体アルファ(PML / RARアルファ)と呼ばれる、これらの前骨髄球性細胞によって作られた融合タンパク質に損傷を与えます。融合タンパク質は、元々別々のタンパク質をコードしていた2つ以上の遺伝子の結合によって作成されたタンパク質です。
APLのATO
ATOは、次のように、急性前骨髄球性白血病(APL)の特定の症例の治療での使用が承認されています。
- 新たに診断された低リスクから中リスクのAPL。これにより、ATOはオールトランスレチノイン酸(ATRA)と組み合わせて使用されます。
- 以前の治療にレチノイドと化学療法が含まれていた人々における、癌細胞の特定の遺伝子変化の存在下での再発/難治性APL-t(15; 17)転座および/または前骨髄球性白血病/レチノイン酸の存在-受容体-アルファ(PML / RAR-アルファ)遺伝子。
プレゼンテーション時、またはAPLの初期評価と診断時の人の白血球(WBC)カウントは、これらのAPLリスクグループを作成するためによく使用されます。これにより、次のカテゴリが使用されます。
- 低リスクまたは中リスクのAPL =初期WBC数≤10,000/ microL;
- 高リスクAPL =初期WBC数> 10,000 / microL。
17歳までの子供におけるATOの安全性と有効性は確立されていません。 5歳未満の子供に関するデータはなく、年長の子供に関するデータは限られています。ある分析では、18歳未満(5〜16歳の範囲)の7人の患者が0.15 mg /の推奨用量でATOで治療されました。 kg /日、5人の患者が完全な反応を達成しました。
ATOに対する他のAMLサブタイプの奏効率は調べられていません。 ATOによる研究は進行中であり、将来的には、癌の治療におけるこの薬剤のさまざまな追加の用途があるかもしれません。
誘導療法としてのATO + ATRA
APLの治療法は、他の種類のAMLの治療法とは異なります。誘導として知られる治療の最初のステップは、寛解をもたらすことを目的とし、APLの異常な細胞である前骨髄球をより正常な細胞に成長させることを含みます。
オールトランスレチノイン酸(ATRA)は、悪性前骨髄球を好中球に成熟させるため、誘導によく使用される非化学療法薬です。これはビタミンAに関連する化合物です。ただし、ATRAだけでは一般に寛解を誘導するのに十分ではありません。つまり、ATRAだけでの寛解は短命で、数か月しか続かない傾向があります。 。
したがって、ATRAは通常、他の薬剤と組み合わせて、APLの患者に寛解を誘導します。アントラサイクリンベースの化学療法と組み合わせたATRAは、最も広範な臨床経験と最大量のデータが存在する標準的な治療法です。
ただし、標準的なアントラサイクリンベースの化学療法の代わりに、ATRAでATO(利用可能な場合)を使用することにはかなりの関心があります。当初、これはアントラサイクリンベースの化学療法に耐えられなかった人々のための選択肢と見なされていました。しかし、最近の臨床試験データは、ATRA + ATOの組み合わせが、適切な患者タイプにおいて、ATRAと化学療法を組み合わせた標準的なレジメンと同じくらい良い結果を生み出す可能性があることを示唆しています。
ATRA + ATOデータのほとんどは、人々が低リスクAPLと中リスクAPLを持っていた研究から来ています。高リスクAPLの患者において、ATRA + ATOがATRA +化学療法とどのように比較されるかについて入手できる情報はほとんどありません。
統合療法
他のタイプのAMLと同様に、APLの患者は、最初の導入療法が完了した後、追加の治療を受け続けます。この後の治療は、地固め療法として知られています。
使用される特定の薬物療法は、導入療法としてどのような治療が行われたかに一部依存します。統合療法の例は次のとおりです。
- 数サイクルのアントラサイクリン+ ATRA(異なるサイクルで異なるアントラサイクリンが使用される場合があります)
- アントラサイクリン+シタラビンを少なくとも2サイクル
- 約75日間で2サイクルのATO、次に2サイクルのATRA +アントラサイクリン
- 数サイクルのATRAとATO
メンテナンス療法
APLの一部の患者では、強化の後にATRAによる維持療法が少なくとも1年間続く場合があります。低用量の化学療法薬である6-メルカプトプリン(6-MP)とメトトレキサートも投与されることがあります。
他の疾患部位のATO—予備調査
APLの治療におけるATOの成功は、他の悪性腫瘍の治療におけるATOの潜在的な役割への科学的関心に拍車をかけました。
多くの場合、研究は非常に予備的なものであり、「試験管と動物の研究」に限定されることもありますが、ATOがこのようなさまざまな異なる疾患部位と設定で調査されているという事実は、それ自体が注目に値します。
これらのさまざまな研究の方向性のサンプルを次に示します。
結腸がんからの肺転移
養子T細胞療法は、免疫系が癌や他の病気と戦うのを助けるために使用される治療法です。 T細胞は患者から収集され、実験室で増殖して免疫系の反応が成功する確率を最大化し、その後、癌と戦うために患者に戻されます。
王と同僚による動物研究でオンコターゲット、細胞傷害性T細胞と組み合わせたATOは、結腸癌の肺転移モデルにおいて相乗効果と生存期間の延長をもたらしました。 Wangらは、養子T細胞療法の成功は、制御性T細胞の減少に起因することが多く、ATOはこれらの細胞を枯渇させることによってプラスの効果をもたらす可能性があると指摘しました。
肝臓がんからの肺転移
APLでのATOの成功を考えると、研究者たちはATOが肝癌で同様の効果をもたらすのではないかと考えました。 Luらの報告によると、ATOの注入は肝癌の腫瘍増殖を阻害することが示されています。
さらに、ATOは、関連する癌性疼痛を伴う肝臓癌からの肺転移の治療に効果的な薬であると報告されています。Luらは、ATOがRhoCと呼ばれるタンパク質を阻害することにより、肝がん細胞の浸潤と転移を阻害できること、およびRhoCとその「クシン分子」であるエズリンがATOの抗腫瘍機能に関与している可能性があることを研究が示していると述べました。 。
したがって、彼らは、ATOによる転移性肝癌細胞の阻害のメカニズムを研究することを目的とした。彼らは、ATO治療前後のエズリンの発現パターンを観察の窓として使用し、ATO治療が肝癌におけるエズリンの発現を有意にダウンレギュレートできることを発見しました。
多形性膠芽腫
多形性膠芽腫(GBM)は、急速に成長する侵攻性の脳腫瘍です。これは、テッドケネディの命を奪ったタイプの癌であり、ジョンマケイン上院議員が2017年に診断されたものです。
三酸化ヒ素は、臨床的に安全な用量(1〜2μM)のGBMを含む多種多様な固形腫瘍の増殖を阻害するが、退行させることはないと報告されています。吉村らは、低濃度(2μM)の三酸化ヒ素がGBM細胞の分化を誘導し、マウス研究で組み合わせて使用すると他の抗がん療法の効果を高める可能性があることを指摘しました。将来のGBM療法のために。
骨肉腫
骨肉腫は一般的な骨肉腫であり、治癒率は過去25年から30年の間あまり変化していません。
オートファジーと呼ばれるプロセスとは、細胞のリソソームが分解してタンパク質凝集体や損傷した細胞小器官を排除することを指します。基本的には、細胞の細胞質をきれいに保つためにゴミを取り出します。
オートファジー調節は骨肉腫の潜在的な治療戦略と考えられており、以前の研究では、ATOが有意な抗発癌活性を示すことが示されていました。
Wuらは最近、ATOが実験的ヒト骨肉腫細胞(細胞株MG-63)のオートファジー活性を増加させることを示しました。興味深いことに、オートファジーのブロック(薬物または遺伝子工学を使用)減少ATOが誘導する細胞死は、ATOがMG-63細胞のオートファジー細胞死を引き起こすことを示唆しています。
Wuらは、次のように結論付けています。「これらのデータを総合すると、ATOは、ROS-TFEB経路を介して媒介される過剰なオートファジーを誘発することにより骨肉腫細胞死を誘発することが示されています。本研究は、骨肉腫におけるATO治療の新しい抗腫瘍メカニズムを提供します。」
ベリーウェルからの一言
過去30年間で、APLは非常に致命的な病気から非常に治癒可能な病気になりました。 ATRA、化学療法、そして最近ではATOによる治療戦略は、これらの進歩に役立つと考えられています。
しかし、これらの進歩により、まだいくつかの「未解決の領域」があります。ここでは、ATO + ATRAの長期データが良好であると報告されていますが、ATOの長期的な安全性と有効性を検討することができます。別の未解決の領域は、ATRA / ATOの時代に好まれる維持療法である可能性があります。