Novavaxは、メリーランドを拠点とするバイオテクノロジー企業であり、コロナウイルス病2019(COVID-19)に対するワクチンの開発に従来のアプローチを採用しています。同社は、ワクチン候補であるNVX‑CoV2373の第3相試験を9月に英国で開始し、2回目の第3相試験を米国とメキシコで12月に開始しました。これらの2つの後期試験には、合計で約45,000人の参加者が登録されます。
これによりNovavaxは競合他社に遅れをとっていますが、ワクチン試験の最初の結果は有望です。
zoranm /ゲッティイメージズ使い方
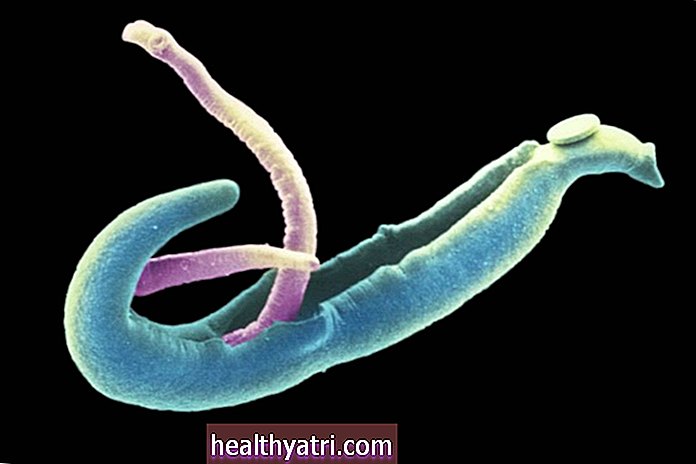
Novavaxワクチンは、新規コロナウイルスの天然スパイクタンパク質を模倣するカスタムメイドのスパイクタンパク質を使用しています。 Novavaxは、組換えナノ粒子技術の開発に長年取り組んでおり、春にこの方法を使用して最初のCOVID-19ワクチンを作成しました。夏までに、初期の臨床試験はワクチンが安全であるように思われることを示しました、そしてより進んだ試験は合衆国と他の国で計画段階に入りました。
2回接種ワクチンは、抗体応答を促すタンパク質を導入することで機能します。これにより、将来のコロナウイルスがヒト細胞に結合する能力がブロックされ、感染が防止されます。このタンパク質は、タンパク質抗原によって誘発される免疫応答を強化するのに重要なNovavaxのMatrix-Mアジュバントと組み合わされています。
それはどれくらい効果的ですか?
Novavaxが発表した初期のワクチン試験の結果は、動物におけるワクチンに対する強い抗体反応を明らかにしました。 2020年8月までに、初期のヒト試験では、重篤な有害事象はなく、副作用もほとんどない強力な抗体反応が示されました。
1月下旬、Novavaxは、英国の第3相試験のデータを予備分析したところ、ワクチンの有効性は89.3%であり、英国のバリアントB.1.1.7からの保護が含まれていることを発表しました。同社はまた、南アフリカでの第2b相臨床試験でワクチンが60%有効であり、南アフリカの亜種B.1.351からの保護が含まれていることを発表しました。
すべての後期臨床試験の結果は2021年に期待されています。
Novavaxの試験では、参加者はウイルスに直接さらされることはありませんが、代わりに研究者は自然感染アプローチを使用します。課題は、ワクチンまたはマスキングや社会的距離のような他の保護手段が最も保護を提供したかどうかを判断することです。
いつ利用可能になりますか?
Novavaxのワクチン候補は、初期の動物実験データが鼻腔でのコロナウイルスの複製を防ぐのに非常に効果的であることを示したため、多くの関心を集めています。これは、感染率と感染率の両方を減らすのに役立つ可能性があるため、COVIDワクチンの重要な開発です。 。しかし、これは人間の研究ではまだ確立されていません。
ただし、Novavaxは臨床試験に関して競合他社に遅れをとっているため、試験で引き続き成功したとしても、ワクチンは2021年後半まで入手できない可能性があります。同社はまだ配布日の見積もりを発表していません。 2019年はNovavaxにとって困難な年だったため、会社自体も大きな課題に直面しています。理科雑誌は、同社が製造施設の一部を売却し、ワクチンの多くを製造するためにより多くの請負業者に頼らなければならないと報告しました。これにより、生産が遅れる可能性があります。
ワクチンの価格に関する情報はまだ提供されていません。
COVID-19ワクチン:どのワクチンが利用可能で、誰がそれらを入手できるか、そしてそれらがどれほど安全であるかについて最新の状態に保ちます。
Novavaxワクチンは誰が入手できますか?
他のCOVID-19ワクチン候補と同様に、Novavaxワクチンは18歳以上の成人でテストされています。同社は、子供と10代の若者の試験に関する最新情報を提供していません。特定のグループの懸念に関する情報はまだ提供されていません。
研究グループの人口に関係なく、COVIDワクチンを接種できるのは、主に食品医薬品局(FDA)による規制上の決定です。配布中の適格性は、州レベルおよび米国疾病予防管理センター(CDC)によって決定されます。
CDCはワクチン接種の取り組みを主導しており、COVID-19ワクチンのすべての注文は、製造元に関係なく、代理店を経由します。 CDCはワクチンの配布も監督しています。 CDCの予防接種実施諮問委員会(ACIP)は、ワクチン供給の優先順位付け方法について勧告を行っています。
医療従事者と介護施設に住む人々は、認可されたCOVID-19ワクチンを最初に受けました。 CDCによると、米国には1,800万人以上の医療従事者がおり、約130万人のアメリカ人が介護施設に住んでいます。これらの人々はそれぞれ、認可されたワクチンを2回接種する必要があります。これまでのところ。
CDCは、ワクチンの供給が需要に追いつくまでに数か月かかると見積もっています。誰がワクチンを接種するか、そしていつ供給が利用可能になったときに決定されるかについてのガイダンス。米国だけでも人口は約3億3000万人です。つまり、他のワクチンが2回のワクチン接種に続く場合、アメリカ全土にワクチンを接種するには7億回近くのワクチン接種が必要になります。
誰もがいつワクチンを受け取るか、どこでワクチンを入手できるかについての詳細についてはほとんど情報がありませんが、州および地方の保健部門は、ワクチンが利用可能になったときにワクチンの投与量を配布する取り組みを調整します。ワクチンは、診療所と他のワクチンを投与する薬局のような小売店の両方で入手できる必要があります。
ワクチンが利用可能になると、米国政府が購入した用量はすべて市民に無料で提供されます。ワクチン自体は無料ですが、ワクチンを提供する施設や機関は管理費を請求する場合があります。公衆衛生プログラムと保険プランは、COVID-19ワクチン接種に関連する費用を患者に払い戻すことが期待されていますが、情報はまだ提供されていません。
副作用と有害事象
Novavaxワクチンの初期の試験では重篤な有害事象は報告されていませんが、後期の試験結果が発表された後、より多くの情報が利用可能になります。フェーズ3では、有害事象は「低レベルで発生し、ワクチン群とプラセボ群の間でバランスが取れていました」。 Novavaxによると。
資金調達と開発
Novavaxは、COVID-19ワクチンを開発する取り組みに対して、世界で20億ドル以上を授与されており、米国政府だけで16億ドルが授与されています。米国の資金は、オペレーションワープスピードの一部として、および生物医学先端研究開発局(BARDA)から提供されました。 BARDAは、米国保健社会福祉省に該当するプログラムです。そのプログラムとオペレーションワープスピードは、COVID-19と戦うためのワクチンを開発し、使用を承認するまでの時間を短縮することを目指しています。